La esclerosis múltiple (EM) es una enfermedad consistente en la aparición de lesiones desmielinizantes, neurodegenerativas y crónicas del sistema nervioso central.
Actualmente se desconocen las causas que la producen aunque se sabe a ciencia cierta que hay diversos mecanismos autoinmunes involucrados.
Sólo puede ser diagnosticada con fiabilidad mediante una autopsia post-mortem o una biopsia, aunque existen criterios no invasivos para diagnosticarla con aceptable certeza.
Los últimos internacionalmente admitidos son los criterios de McDonald.1
Por el momento se considera que no tiene cura aunque existe medicación eficaz y la investigación sobre sus causas es un campo activo de investigación.
Las causas exactas son desconocidas. Puede presentar una serie de síntomas que aparecen en brotes o que progresan lentamente a lo largo del tiempo. Se cree que en su génesis actúan mecanismos autoinmunes.
Las causas exactas son desconocidas. Puede presentar una serie de síntomas que aparecen en brotes o que progresan lentamente a lo largo del tiempo. Se cree que en su génesis actúan mecanismos autoinmunes.
Se distinguen varios subtipos de esclerosis múltiple y muchos afectados presentan formas diferentes de la enfermedad con el paso del tiempo.
A causa de sus efectos sobre el sistema nervioso central, puede tener como consecuencia una movilidad reducida e invalidez en los casos más severos. Quince años tras la aparición de los primeros síntomas, si no es tratada, al menos 50% de los pacientes conservan un elevado grado de movilidad. Menos del 10% de los enfermos mueren a causa de las consecuencias de la esclerosis múltiple o de sus complicaciones.
Es, tras la epilepsia, la enfermedad neurológica más frecuente entre los adultos jóvenes (desde la casi completa erradicación de la poliomielitis) y la causa más frecuente de parálisis en los países occidentales.
Afecta aproximadamente a 1 de cada 1000 personas, en particular a las mujeres. Se presenta cuando los pacientes tienen entre 20 y 40 años.
Se caracteriza por dos fenómenos:
Aparición de focos de desmielinización esparcidos en el cerebro y parcialmente también en la médula espinal causados por el ataque del sistema inmunitario contra la vaina de mielina de los nervios.
Las neuronas, y en especial sus axones se ven dañados por diversos mecanismos (ver más adelante)
Como resultado, las neuronas del cerebro pierden parcial o totalmente su capacidad de transmisión, causando los síntomas típicos de adormecimiento, cosquilleo, espasmos, parálisis, fatiga y alteraciones en la vista.
En la variante Remitente-Recurrente también se ha detectado inflamación en el tejido nervioso y transección axonal, o corte de los axones de las neuronas, lo que hace que las secuelas sean permanentes.

No existe cura para la esclerosis múltiple. Sin embargo se han encontrado varios medicamentos que son eficaces en su tratamiento, frenando el desarrollo de la enfermedad y combatiendo los síntomas.
Sólo la variante remitente-recurrente tiene tratamientos aprobados por la FDA y la EMEA. Actualmente , son tres interferones (Avonex, Betaseron -conocido en Europa como Betaferon- y Rebif), un conjunto de polipéptidos llamado Copaxone, un inmunosupresor llamado Mitoxantrone y finalmente un anticuerpo monoclonal llamado Natalizumab y comercializado como Tysabri.
Es muy importante, igualmente, la evaluación por parte de un neuropsicólogo para poder abordar cualquier déficit cognitivo que pudiera instaurarse.
Medicamentos experimentales y terapias alternativas se describen en el artículo Tratamiento de la esclerosis múltiple. El estado de las terapias experimentales, llamadas "pipeline", pueden ser consultadas en sitios especializados.
Otra de las posibles vías para el tratamiento de la esclerosis múltiple es el Concepto Bobath.
Epidemiología
Se considera que la esclerosis múltiple aparece cuando se da una combinación de factores ambientales en personas genéticamente predispuestas a adquirirla.
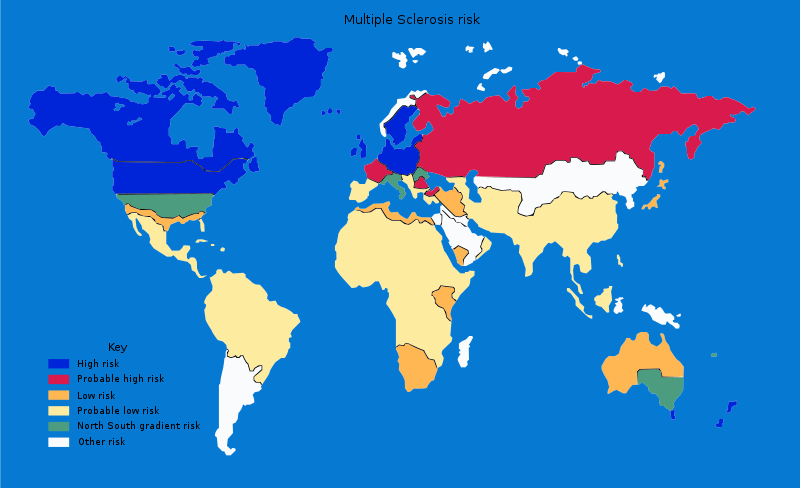
En Europa del norte, América del Norte continental y Australasia uno de cada 1000 personas sufren esclerosis múltiple. En Europa Central es la enfermedad inflamatoria del sistema central nervioso más común. En cambio, en la Península Arábica, Asia, América Central y América del Sur continental la frecuencia es mucho menor. En el África Subsahariana es extremadamente rara.
Con excepciones importantes, hay un gradiente norte-sur en el hemisferio norte y sur-norte en el hemisferio sur, con las menores frecuencias en las zonasecuatoriales. En España este gradiente Norte-Sur se mantiene, la prevalencia media de la península ibérica se puede cifrar en 40-50 casos por cada 100.000 habitantes.
El clima, la dieta, el geomagnetismo, toxinas, la luz solar, factores genéticos y enfermedades infecciosas han sido propuestos como posibles causas de estas diferencias regionales.
Se ha postulado que algún factor medioambiental en la infancia podría tener un papel importante en el desarrollo de la esclerosis múltiple en la vida del adulto.
La teoría se basa en varios estudios sobre personas que han migrado, demostrándose que, si la migración ocurre antes de los 15 años, el inmigrante adquiere la susceptibilidad a la esclerosis de la región a la que se ha desplazado.
Si el desplazamiento ocurre después de los 15 años, la persona mantiene la susceptibilidad de su país de origen. Sin embargo, la enfermedad no se transmite directamente como se ha demostrado en estudios con niños adoptados.
Los primeros síntomas suelen aparecer en personas entre los 20 y los 40 años. Rara vez por debajo de los 15 o por encima de los 60, aunque en las personas mayores no suele detectarse. Como es el caso de muchas enfermedades autoinmunes, es dos veces más común entre mujeres que entre hombres.
Entre los niños, que rara vez desarrollan la enfermedad, la proporción puede llegar a tres niñas por cada niño. En los casos de personas de más de 50 años suele tratarse de hombres.
Según una investigación de Anne-Louise Ponsonby de la der Australian National University en Canberra, la probabilidad de enfermar es tanto menor cuanto más tiempo se haya convivido con los hermanos. Más de cinco años de contacto reducen el riesgo un 90%.
La científica explica el fenómeno por el contagio mutuo de enfermedades infecciosas entre hermanos, lo que protege de las enfermedades autoinmunes.
Factores genéticos
La esclerosis múltiple aparece principalmente en caucásicos. Es 20 veces menos frecuente entre los inuit deCanadá que entre los demás canadienses que viven en la misma región. También es rara entre las tribus indias americanas de América del Norte, los aborígenes australianos y los maorí de Nueva Zelanda. Estos ejemplos señalan que la genética tiene un papel importante en el desarrollo de la enfermedad.
La esclerosis múltiple no es una enfermedad hereditaria. Sin embargo, la enfermedad está influenciada por la constitución genética del individuo y se ha demostrado que existen genes que están relacionados con un mayor riesgo de contraer la enfermedad.
Estos genes, que están siendo estudiados, no son suficientes para diagnosticar la enfermedad.
En general, uno de cada 25 hermanos de un individuo con la enfermedad también se verá afectado. Si un gemelo univitelino se ve afectado, existe hasta un 50% de probabilidad que el otro gemelo también enferme.
Pero sólo uno de cada 20 gemelos bivitelinos se verá afectado si su hermano ha enfermado. Si uno de los padres está afectado por la enfermedad, cada uno de los hijos tendrá una probabilidad de 1 entre 40 de desarrollarla de adulto.
Dos estudios realizados en Canadá y Gran Bretaña muestran la siguiente tabla de probabilidades de enfermar según el grado de parentesco:
Grado de parentesco
|
Probablilidad de enfermar
| |
En la población
|
~ 0,2 %
| |
Familia en 1er grado
|
~ 3 %
| |
Familia en 2o grado
|
~ 1 %
| |
Familia en 3er grado
|
~ 0,9 %
| |
Gemelos univitelinos
|
~ 35 %
| |
Hermanos
|
~ 4 %
|
Diagnóstico
El diagnóstico de la esclerosis múltiple es complejo. Se requieren evidencias de una diseminación de lesiones tanto temporal como espacialmente en el sistema nervioso central. Eso quiere decir que, no sólo tiene que haber por lo menos dos lesiones distintas verificables por síntomas clínicos o por resonancia magnética, además tiene que haber evidencias de nuevos síntomas o lesiones en un intervalo de 30 días.
Una muestra de líquido cerebroespinal obtenida con una punción lumbar sirve para obtener pruebas de la inflamación crónica en el sistema nervioso, a menudo indicada por la detección de bandas oligoclonales (moléculas de anticuerpos) en el líquido.
Los estudios de conductividad nerviosa de los nervios óptico, sensoriales y motores también proporcionan pruebas de la existencia de la enfermedad, ya que el proceso de desmielinización implica una reducción de la velocidad de conducción de las señales nerviosas. El estudio se realiza comparando los tiempos de reacción con mediciones preestablecidas.
El proceso de diagnóstico se completa con la realización de pruebas para excluir otras enfermedades que pueden imitar a la esclerosis como la Enfermedad de Devic, la sarcoidosis, la vasculitis y la enfermedad de Lyme.
Síntomas
Las lesiones del sistema nervioso central que causan la EM no siempre se manifiestan directamente como síntomas clínicos detectables y claramente atribuibles a la enfermedad, por lo que en ocasiones se tiende a restar importancia a los primeros signos. Sin embargo, el origen de la EM ya está presente y comienza a progresar.
Aunque en algunas ocasiones al principio de la EM se acumula poca discapacidad y la calidad de vida no se ve demasiado afectada, la realidad es que el sustrato de la enfermedad ya se está desarrollando.
Existen abundantes evidencias clínicas y científicas que indican que, de lo que ocurra en las fases iniciales de la EM , depende en gran medida su evolución posterior.
En otras palabras, las lesiones de hoy en el sistema nervioso central, son la causa de la discapacidad de mañana; de modo que si no se previenen hoy, mañana será demasiado tarde para conseguir la recuperación. Resulta clave detectar la EM cuanto antes, para poder actuar a tiempo.
Normalmente, la Esclerosis Múltiple se detecta tras un primer brote de la enfermedad. Los síntomas de este primer brote son muy variados, pero entre los más fácilmente reconocibles, destacan hormigueo, debilidad, falta de coordinación (ataxia), alteraciones visuales, rigidez muscular, trastornos del habla (disartria), andar inestable, entre otros. No en todos los pacientes se manifiestan todos los síntomas ni durante el mismo tiempo.

Tras detectar estos síntomas es fundamental acudir al médico para realizar las pruebas oportunas. En la actualidad, aunque no existe ninguna prueba de laboratorio que de manera aislada permita confirmar o eliminar por completo la posibilidad de padecer EM, la tecnología disponible, particularmente la resonancia magnética, el análisis del líquido cefalorraquídeo y los potenciales evocados, sí permiten un alto grado de seguridad en el diagnóstico, incluso antes de que haya una confirmación clínica de la enfermedad.
Si se detecta que los síntomas son provocados por la Esclerosis Múltiple , el neurólogo podrá iniciar un tratamiento adecuado para que los brotes tarden más en aparecer y sus efectos sean menores.
Se ha demostrado que el tratamiento precoz reduce significativamente el número de brotes y la intensidad de los mismos.
Las personas afectadas pueden manifestar un amplio número de síntomas, pero varían mucho de unas a otras, tanto en el tipo de síntomas como en su grado.
En principio, pueden clasificarse según la zona del sistema nervioso afectada en: derivados del daño al nervio óptico, derivados del daño a la médula espinal (en concreto, los relativos a la movilidad son de este tipo) y derivados del daño al cerebro.
Se presentan a continuación los más comunes:
Astenia (fatiga)
Disfagia (problemas al tragar)
Disartria (problemas de habla)
Disnea (problemas al respirar)
Espasticidad (rigidez muscular)
Fasciculaciones musculares (pequeñas pero generalizadas vibraciones musculares)
Problemas de visión: pérdida, doble visión, nistagmo
Problemas congnoscitivos: dificultad de realizar tareas simultáneas, de seguir instrucciones detalladas, pérdida de memoria a corto plazo, depresión.
Labilidad emocional (risas y llantos inapropiados sin afectación psicológica)
Estreñimiento secundario a inmovilidad.
Sintomatología cognitiva
Si bien antiguamente se consideraba que no existían déficits cognitivos en el EM, sino que era una enfermedad fundamentalmente física; actualmente se sabe que es común un patrón de déficits cognitivos específicos.
El patrón que siguen los déficits cognitivos es un patrón fronto-subcortical; afectando por tanto a las funciones localizadas en el lóbulo frontal y en las zonas subcorticales.
Respecto a los déficits frontales puede haber cambios conductuales (apatía, falta de motivación, pseudodepresión; o por el contrario desinhibición, impulsividad, agresividad e irascibilidad, infantilismo...) y en las funciones ejecutivas (Capacidad para planificar, flexibilidad mental, razonamiento...)
En cuanto a las funciones subcorticales lo más habitual es que exista una reducción en la velocidad de procesamiento cognitivo. Estos déficits deben ser evaluados por un neuropsicólogo (neuropsicología) y existen evidencias parciales sobre que la rehabilitación neuropsicológica específica puede ayudar a reducirlos o compensarlos.

Aspectos emocionales
Dado que la esclerosis múltiple afecta el cerebro y la espina dorsal, es de naturaleza degenerativa y a menudo lleva a una discapacidad progresiva, no es extraño que las personas afectadas sufran dificultades emocionales. Depresión, ansiedad, ira, miedo, junto con otras emociones se diagnostican a menudo entre las personas que sufren EM o los allegados.
A pesar de que estos sentimientos son comprensibles, tienen implicaciones sociales, especialmente cuando interfieren con el trabajo, la escuela y la vida familiar. En particular, la depresión lleva asociada el peligro de suicidio.
Todos estos problemas pueden ser solucionados con tratamientos psicológicos y medicación adecuada.
Depresión
La depresión en estos casos puede originarse tanto en las implicaciones del diagnóstico como en los efectos que produce la enfermedad en el cerebro. El cerebro es un órgano altamente especializado y es el origen de todas las emociones. Cuando un brote afecta la parte del cerebro en que se procesan las emociones, el resultado puede incluir depresiones.
También se ha informado de casos de depresión en algunos pacientes que toman interferón beta (Avonex® o Rebif®) para tratar la enfermedad.
Ansiedad
La ansiedad también es un problema frecuentemente asociado con la EM. Al igual que la depresión, puede estar originada por la enfermedad o por las implicaciones del diagnóstico.
Las consecuencias cognitivas de la EM también suelen estar asociadas a la EM. No es raro que personas que sufren la enfermedad desarrollen falta de memoria, dificultades en explicar conceptos abstractos, organizar, planificar u olviden determinadas palabras. Estos síntomas pueden generar ansiedad y resultar en una retirada de la vida social.
Otras alteraciones
La ira es otro sentimiento que puede ir asociado a la EM y, de hecho, con todas las enfermedades crónicas graves. También se ha informado de la aparición de "risa patológica" y "llanto patológico". Esencialmente se refiere a una reacción inapropiada a la situación, tal como risas en un funeral o llanto al oír buenas noticias. A menudo es consecuencia de la desmielinización de las áreas del cerebro encargadas del juicio.
Curso y formas de la enfermedad
En la mayoría de los casos la esclerosis comienza con la aparición aguda de síntomas en un espacio que varía de horas a días, habitualmente llamado exacerbación, ataque o episodio.
Más adelante se habla de recaída. El primer síntoma es a menudo la neuritis óptica, una inflamación del nervio óptico que causa deterioro de la visión y dolor al mover el ojo. Sin embargo, no todos los pacientes con una neuritis óptica desarrollan EM. Alteraciones sensoriales como entumecimiento u hormigueotambién son síntomas iniciales frecuentes.
En principio, la esclerosis puede comenzar con cualquiera de los síntomas asociados a la enfermedad.
EM benigna En los casos de EM benigna, tras uno o dos ataques, la recuperación es completa. La enfermedad no empeora a lo largo del tiempo y suele tener síntomas menos graves.
Estos casos sólo se identifican cuando queda una incapacidad permanente pequeña a los 10 o 15 años del primer ataque, que fue identificado en su día como EM con recaídas.
EM con recaídas y remisiones Especialmente en fases tempranas de la enfermedad, los síntomas disminuyen o desaparecen espontáneamente en un período que puede durar de días a meses.
Este tipo de transcurso se llama con recaídas y remisiones. Nuevas recaídas pueden aparecer en semanas o varios años y son imprevisibles. Estas recaídas pueden incluir los síntomas anteriores y/u otros nuevos. Sin embargo, estudios de resonancia magnética muestran que el daño a los nervios puede continuar en estos pacientes incluso cuando los síntomas han remitido. Se sabe desde hace mucho tiempo que la EM nunca duerme, por lo que la importancia del tratamiento preventivo es grande. Muchos enfermos permanecen en esta fase el resto de sus vidas.
EM progresiva secundaria
En muchos casos la enfermedad cambia al cabo de varios años y los síntomas comienzan a progresar lentamente con o sin recaídas sobreimpuestas. No se conoce aun bien su etiología
EM progresiva primaria
Un 10 % de todos los individuos afectados presentan un avance crónico desde el principio sin remisión de los síntomas. Es la llamada forma progresiva primaria y a menudo aparece junto a debilidad en las piernas y alteraciones en el andar y en la vejiga urinaria.
Parece que son procesos degenerativos y no inflamatorios los que tienen un papel preponderante en este tipo. En los casos en que la forma progresiva primaria se sobreimponen a recaídas se suele hablar de progresiva con recaídas.
Existen también otras formas de esclerosis múltiple, que para muchos son enfermedades distintas, que se agrupan bajo el nombre colectivo de formas frontera de la esclerosis múltiple.
Los orígenes de la enfermedad son desconocidos.
Se ha lanzado la hipótesis de que puede ser producida por una combinación de varios factores genéticos y medioambientales.
Esto incluye posibles infecciones virales u otros factores en la niñez o durante el embarazo que puedan preparar el sistema inmunitario para una reacción anormal más tarde.
A nivel molecular, puede que exista una similitud estructural entre una agente infeccioso desconocido y componentes del sistema nervioso central, lo que causaría confusión más tarde en el sistema inmunitario (un proceso llamado mimetismo molecular). Con todo, aún no se conoce ningún virus de la esclerosis. Desde luego, la esclerosis múltiple no es contagiosa.
Otras hipótesis propuestas intentan establecer relaciones con enfermedades vasculares.
Recientemente ha sido propuesta una relación con una enfermedad vascular conocida como insuficiencia venosa cerebroespinal crónica.3
Fisiopatología
Los tejidos del sistema nervioso y de la médula espinal están protegidos por un sistema de vasos capilares, llamado barrera hematoencefálica, que en los pacientes de esclerosis múltiple no funcionan. Por causas desconocidas, macrofagos y linfocitos pueden cruzar las barreras hematoencefálicas de estos pacientes y comenzar un ataque autoinmune.
Se ha conseguido reconstruir el proceso del ataque del sistema inmunitario a la mielina a partir de observaciones en los tejidos dañados y el estudio de la Encefalomielitis Experimental Autoinmune (o EAE, de sus siglas en inglés), que es una enfermedad similar a la EM que puede ser inducida en los roedores.
Tipos de lesiones
Recientemente la National MS society americana ha lanzado un proyecto llamado The lesion project para catalogar todos los tipos de lesiones posibles y desarrollar un modelo más preciso de como ocurren las cosas.
Se han encontrado cuatro familias de lesiones diferentes pero no hay un consenso en cuanto al significado de este hecho. Unos piensan que esto significa que la EM es realmente una familia de enfermedades. Otros piensan que las lesiones pueden cambiar de un tipo a otro con el tiempo o según el individuo.

Las cuatro familias o "patterns" son los siguientes:

Las cuatro familias o "patterns" son los siguientes:
Patrón I: La lesión presenta células T y macrofagos alrededor de vasos capilares. Los oligodendrocitos están más o menos intactos y no hay signos de activación del sistema inmune complementario (anticuerpos)
Patrón II: La lesión también presenta células T y macrófagos alrededor de los capilares. Los oligodendrocitos también se preservan, pero aparencen signos de activación del complemento.
Patrón III: Las lesiones son difusas y presentan inflamación. Los oligodendrocitos presentes están dañados (oligodendrogliopatía distal). Hay también signos de activación de la microglia y pérdida de MAG (proteína constituyente de la mielina, del inglés myelin associated glycoprotein). Las lesiones no rodean los vasos capilares y hay un anillo de mielina intacta alrededor de ellos. También aparece una remielinización parcial y apóptosis de oligodendrocitos.
Patrón IV: La lesión presenta bordes abruptos y oligodendrocitos degenerados, con un anillo de mielina. Ausencia de oligodendrocitos en el centro de la lesión. No está activado el complemento ni hay perdida de MAG.
Los dos primeros patrones se consideran ataques autoinmunes contra la mielina y los dos últimos contra los oligodendrocitos. Los dos primeros patrones son además similares a los producidos en EAE.

Las formas limítrofes de la esclerosis múltiple también presentan lesiones incluidas en estos patrones. Así la neuromielitis óptica tendría lesiones mediadas por activación de complemento (patrón II). La esclerosis concéntrica de Baló mostraría pérdida de MAG según el patrón III y la EM progresiva primaria se correlacionaría con el patrón IV
Desmielinización
En estado normal, existe una barrera entre el sistema nervioso central y la sangre llamada barrera hematoencefálica, que está formada por células endoteliales tapizando las paredes de los vasos sanguíneos. Por causas desconocidas, en los pacientes de esclerosis esta barrera no funciona bien, y las células T autorreactivas la cruzan. A partir de este momento, estas células T van a atacar la mielina del sistema nervioso, produciendo una desmielinización.
A la vez aparece un proceso inflamatorio. La inflamación es facilitada por otras células inmunitarias y elementos solubles, como la citocina y los anticuerpos. A causa de este comportamiento anormal del sistema inmunitario, la esclerosis múltiple es considerada una enfermedad autoinmunitaria.
Ampliamente aceptado es que un subtipo especial de linfocitos, llamados células CD4-Th1-T, tienen una función clave en el desarrollo de la enfermedad. Bajo circunstancias normales, estos linfocitos pueden distinguir entre células propias y ajenas. En una persona con esclerosis múltiple, sin embargo, las células reconocen partes sanas del sistema central como ajenas y las atacan como lo harían con un virus.
En la esclerosis, la parte atacada es la mielina, una sustancia grasa que cubre los axones de las células nerviosas y que es importante para una transmisión nerviosa adecuada.
La inflamación finalmente lleva a la apertura de la barrera hematoencefálica, lo que puede acarrear problemas como edemas. También causa la activación de macrófagos, de metaloproteinasas y otras proteasas ycitocinas. Finalmente llevará a la destrucción de la mielina, proceso llamado desmielinización.

Daño a los axones
A través de la resonancia magnética y otros sistemas, se ha demostrado que el daño a los axones es una de los principales causas del desarrollo de discapacidades permanentes. Se ha demostrado que esta lesión interviene no sólo en formas crónicas o en estadios tardíos de la enfermedad, sino que está presente desde el inicio.
Los mecanismos que llevan a este tipo de daños no están explicados en su totalidad.
Actualmente parece que una regulación anómala del glutamato así como la liberación de monóxido de nitrógeno (NO) tienen una función importante.
Varios experimentos en animales con EAE, encefalitis inducida, enfermedad supuestamente similar a la Esclerosis múltiple, han mostrado que a los que se les dieron medicamentos para la disminución de los niveles de glutamato en el cerebro tuvieron una disminución significativa en los daños a los axones.
Otra posibilidad es la destrucción directa de los axones por las células T autorreactivas.
Remielinización
Los oligodendrocitos originales que forman la cubierta de mielina no son capaces de recrear la cubierta una vez que ha sido destruida. Sin embargo, el cerebro es capaz de reclutar células madre que migran de otras zonas del cerebro desconocidas, se diferencian en oligodendrocitos maduros y recrean la cubierta de mielina.
Esta nueva cubierta a menudo no es tan gruesa o efectiva como la original y ataques repetidos tendrán como reacción remielinizaciones cada vez menos efectivas, hasta que se forma una placa alrededor de los axones dañados.
Las células madre se diferencian y remielinizan axones in vitro sin ningún problema, por lo que se sospecha que la inflamación o el daño al axón inhiben la diferenciación de las células madre in vivo.
La remielinización es una de las razones por las que, especialmente en la primeras fases de la enfermedad, los síntomas tienden a disminuir o desaparecer después de días a meses.
Resultado
Sin embargo, el daño a los axones y la pérdida irreversible de las neuronas aparecen muy pronto en el transcurso de la enfermedad. Los síntomas de la esclerosis son causados por lesiones múltiples en el cerebro y la espina dorsal y pueden variar mucho entre individuos, dependiendo de dónde ocurran las lesiones.
A pesar de todo, la plasticidad del cerebro a menudo puede compensar una parte del daño.
Datos experimentales indican que nervios dañados pueden también recuperar parcialmente la función a través de la creación de canales de sodio en las membranas celulares.
Factores que provocan una recaída
En general, las recaídas tienden a ocurrir con más frecuencia durante la primavera y el verano que en otoño o en invierno. Infecciones como un catarro, un resfriado o una diarrea aumentan el riesgo de recaída. Sin embargo, la vacuna contra la gripe es inocua y no provoca recaídas como se ha demostrado en diversos estudios recientes. La vacuna del tétanos también se considera inocua, aunque no ha sido estudiada con detalle.
En general, las vacunas con virus vivos atenuados aumentan el riesgo de recaída.
El embarazo puede afectar directamente la probabilidad de recaída. Los últimos tres meses de embarazo ofrecen una protección natural contra la recaída, mientras que los primeros meses y especialmente las primeras seis semanas el riesgo aumenta entre un 20 y un 40%. Según estudios modernos, el embarazo no afecta la incapacidad a largo plazo. La esclerosis múltiple no aumenta la probabilidad de tener un niño disminuido, aunque sí existe la posibilidad de transmisión de la enfermedad (ver sección Genética).
Estadísticamente no hay evidencias de que accidentes u operaciones provoquen recaídas. En principio, la cirugía no precisa de cuidados especiales que no sean causadas por discapacidades existentes.
El estrés puede causar una recaída, aunque los datos de los estudios son inconsistentes.
El calor y el agotamiento pueden aumentar los síntomas temporalmente, fenómeno conocido como síntomas de Uhthoff. Esta es la razón de que algunos pacientes eviten saunas o incluso duchas calientes. Sin embargo, el calor no es un factor demostrado de recaída. Una fuerte exposición al sol debe ser evitada, ya que los rayos ultravioleta son un fuerte estímulo del sistema inmunitario.
Pronóstico
Actualmente no hay pruebas clínicas establecidas que permitan un pronóstico o decidir una respuesta terapéutica, aunque existen investigaciones prometedoras que necesitan ser confirmadas, como la detección de los anticuerpos anti-MOG (anticuerpo sérico contra la glicoproteína de la mielina de los oligodendrocitos,Myelin oligodendrocyte glycoprotein) y anti-MBP (anticuerpo contra la proteína básica de la mielina, Myelin basic protein), como factores predictores de evolución a la enfermedad instaurada.
La incertidumbre es uno de los aspectos psicológicos que resulta más difíciles de llevar en la EM.
Debido a la mejora en el tratamiento de complicaciones como infecciones pulmonares o en la vejiga urinaria, la esperanza de vida de las personas diagnosticadas con EM sólo se ve ligeramente reducida.
Cuanto más joven se es cuando aparece la enfermedad, más lentamente avanza la discapacidad. Esto es debido a que en personas mayores es más frecuente la forma crónica progresiva, con una acumulación mayor de discapacidad.
La discapacidad tras cinco años se corresponde con la discapacidad a los 15 años: 2/3 de los pacientes con EM que tengan poca discapacidad a los 5 años, no se deteriorarán mucho en los 10 años siguientes. Otros casos de EM en la familia no influyen en la progresión de la enfermedad. Uno de cada tres pacientes seguirá siendo capaz de trabajar después de 15 a 20 años.
Pérdida de visión o síntomas sensoriales (entumecimiento u hormigueo) como síntomas iniciales son signos de un pronóstico benigno. Perturbaciones en el andar y cansancio son signos de un pronóstico negativo.
Una rápida regresión de los síntomas iniciales, edad a la que aparece la enfermedad por debajo de los 35, sólo un síntoma inicialmente, desarrollo rápido de los síntomas iniciales y corta duración de la última recaída indican un buen pronóstico.
Si la forma es con recaídas y remisiones, estadísticamente serán necesarios 20 años hasta que la silla de ruedas sea necesaria. Esto quiere decir que muchos pacientes nunca la necesitarán.
Si la forma es progresiva primaria, como media, se necesitará una silla de ruedas tras 6 o 7 años. Hay que tener en cuenta que estos datos a largo plazo fueron tomados antes de la llegada de los medicamentos inmunomoduladores modernos hace unos 10 años. Estos medicamentos consiguen retrasar el progreso de la enfermedad varios años.
Historia
Noticias sobre pacientes
Existen algunos informes antiguos sobre pacientes que pudieran haber tenido esclerosis múltiple. Santa Lidwina de Schiedam (1380 - 1433), una monja holandesa, podría haber sido la primera paciente de la enfermedad conocida. Desde los 16 años, desarrolló dolores intermitentes, debilidad en las piernas y pérdida de visión, síntomas típicos de la esclerosis. Murió a los 53 años.
Augustus Frederick d'Este (1794-1848), un nieto ilegítimo del rey Jorge III de Inglaterra, otro paciente famoso de esclerosis, dejó un diario detallado describiendo sus 22 años de convivencia con la enfermedad. Comenzó a los 28 con una pérdida repentina temporal de la vista, tras el funeral de un amigo. Durante su enfermedad desarrolló debilidad en las piernas, torpeza en las manos, entumecimiento, mareos, alteraciones de la vejiga y disfunción eréctil.
En 1844 se vio confinado a una silla de ruedas. Hasta su muerte cuatro años más tarde, mantuvo una visión optimista de la vida.
W. N. P. Barbellion también escribió un diario detallado de su diagnóstico y su lucha con la enfermedad. El diario se publicó en 1919 como The Journal of a Disappointed Man (El diario de un hombre desilusionado).
Otras personas ilustres que han sufrido la enfermedad son Alberto Santos Dumont, pionero brasileño de la aviación, Heinrich Heine, poeta alemán, Florence Austral, soprano australiana, Ivalio Iordanov, jugador de fútbol búlgaro, Jacqueline du Pré, violoncellista inglesa y Clive Burr, Ex batería de la banda inglesa de Heavy MetalIron Maiden.
En la serie de televisión The West Wing (El ala oeste) al presidente ficticio de los EE. UU., Josiah "Jed" Bartlet, le es diagnosticado esclerosis múltiple. El argumento lleva al presidente a presentar el hecho al público en la ficción, lo que ha contribuido para destruir algunos mitos y educar a los telespectadores sobre la enfermedad.

En 1970 le diagnostícan esclerosis múltiple a Miquel Martí i Pol, famoso escritor poeta catalán.
Investigación clínica
Robert Hooper (1773-1835), un patólogo británico y médico en ejercicio, Robert Carswell (1793-1857), profesor británico de patología, y Jean Cruveilhier (1791-1873), un profesor de anatomía patológica francés, fueron los primeros en describir la enfermedad con ilustraciones médicas y detalles clínicos.
Basándose en esto, Jean-Martin Charcot (1825-1893), un neurólogo francés, resumió los datos anteriores y realizó importantes contribuciones con las observaciones clínicas y patológicas propias. Reconoció la esclerosis múltiple (sclerose en plaques) como una enfermedad distinta y separada.
Tras los trabajos de Charcot, varios investigadores como Eugène Devic (1858-1930), Jozsef Balo (1895-1979), Paul Ferdinand Schilder (1886-1940) y Otto Marburg (1874-1948) encontraron casos especiales de la enfermedad que ahora se conocen como formas limítrofes de la esclerosis múltiple, ya que algunos autores los clasifican como EM y otros no.
Estos casos son un caso clínico especial, Enfermedad de Devic, también conocido como EM óptico-espinal o Neuromielitis óptica, NMO), tres formas patológicas (Esclerosis concéntrica de Balo, Esclerosis de Schilder o difusa y Esclerosis de Marburg, también llamada aguda o maligna), una forma asociada, (neuropatía periférica autoinmune) y una enfermedad asociada (encefalomielitis diseminada aguda o ADEM).
Para ver más:
Federación Españolapara la Luchacontra la Esclerosis Múltiple.
Portal para pacientes de EM y sus familiares
El Parkinson y la esclerosismúltiplese curan... con cirugía.
Un estudio con células madre logra ralentizar el avance dela esclerosis
Estudian el deterioro cognitivo en la esclerosis múltiple
La que escribe con los ojos
Fundación Francisco Luzón Unidos contra la ELA
Detrás de la Campaña.
Francisco Luzón pide un Plan Nacional de Investigación en ELA
Terapia con helmintos




















No hay comentarios:
Publicar un comentario
DEJA TU COMENTARIO